结构化学基础壹
约定:本文用加粗标记定义或概念,实验名称由斜体标注。本文中所有图片均为网图,侵删。
1. 经典核原子模型
1.1 电子的发现
如图,在一个两端各嵌有一个金属电极的玻璃管中施加几千伏特的高压,并将管中气体抽成真空。可以看到荧光屏上出现了一条笔直的荧光带。
给管中是假一个磁场(用磁铁吸引),可以观察到阴极射线发生了弯曲。该电子流具有负电荷。
利用该装置还能测出电子的电荷
1.1.1 测定电子的速度
若电子的电荷为
即:
这样就能算得电子的速度。
1.1.2 测定电子的电荷
1.2 原子模型的发展史
1.2.1 早期的模型
在该实验中,大部分粒子通过了金箔,并没有改变运动方向,少部分粒子发生偏转,更少部分被反弹或原路返回。该实验能够得出以下结论:
- 原子核内部很空旷,中间的有一个原子核且带正电。
- 整个原子的全部质量几乎都集中在这个原子核上。
- 带负电的电子高速在核外绕核转动。
估算金箔原子核的大小:
,其中左边为假定粒子的动能,右边为该粒子最靠近原子时转化成的库伦排斥势能。 分别表示两者的核电荷数( 与 ), 表示该最近的距离。
1.2.2 普朗克量子论
1.2.2.1 黑体辐射实验
绝对黑体是指能全部吸收辐射电磁波的物体(看上去就是完全黑色的,理想化模型),在受热时能发出连续波长的电磁辐射。下图为黑体在不同温度下,电磁辐射波长与强度的关系图像。
由图,虚线表示经典力学中,随着波长减小,辐射强度应该无限增大。然而在实验观测中,当波长进入了紫外区,出现了经典力学无法解释的现象。这就是紫外灾难。
其中,
例题:电磁辐射波长为
的光子能量为多少?
1.2.2.2 光电效应
爱因斯坦使用普朗克量子论解释了该实验,认为光由光子组成,它的能量也是不连续的。用公式来表示,就是:
其中,
由此可见,只有当
波长、波速与频率之间的关系:
,即 。当我们在研究标准的光的时候,可以将光速 带入波速 。
1.2.3 波尔
要点:电子在轨道上,而轨道具有一定的能量。
1.2.3.1
氢原子光谱上各个光的波长可由以下经验公式得出。其中
进而可以计算波数:
1.2.3.2 原子的轨道能量
其中,
当
离原子核越近,能量越低,越稳定。电子层(又称能层),从里到尾分别是
, , , 。
1.3 微观粒子的波粒二象性
波粒二象性,指微粒既具有波动性又具有微粒性。并且这样的微观粒子不可能同时准确测定位置和动量,即测不准性或不确定性。
- 光的波性:干涉、衍射现象;
- 光的粒性:发射、吸收、光电效应。
1.3.1 爱因斯坦质能方程
当我们认为光子是粒子时,就可以认为它具有的能量为
然而,光又是波。故
求得动量:
电子的波长也就可以求得:
在等式
1.3.2海森堡不确定原理
在宏观世界中,
2. 薛定谔方程(简化版)
笔者只也只会介绍薛定谔方程中的几个参数,用以解释现代原子轨道理论。
2.1 前置技能
2.1.1 概率密度与电子云
在上一节的“海森堡不确定原理”中,我们已经知道了在微观世界中,粒子是难以预测的,所以之前波尔所提出的电子在轨道上运动,就显得有些问题了。电子的运动是不确定的、无法预测的,它不一定就在某个轨道上乖乖运动。那么,科学家们又该如何进一步研究呢?
实际上,我们并非非得要算出电子的运动轨迹。我们只要统计电子在各个位置的分布,就能大概了解电子的运动情况。
在一个空间中,我们定义概率密度
随后,我们将这个概率密度形象地表示在一个三维空间中,便得到了电子云(概率密度分布图)。
再将空间出现概率
2.1.2 波函数
2.1.3 径向分布图像
对于某个轨道,
该图的物理意义是,单位厚度球壳内电子的分布概率。
2.2 方程的参数
2.2.1 主量子数
表示轨道离原子核的远近(决定了电子能级)。
可以取任意正整数,表示是第几层的轨道。
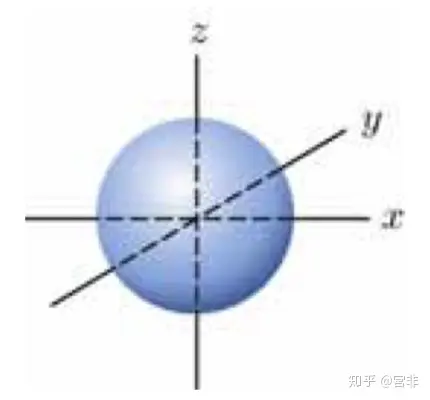
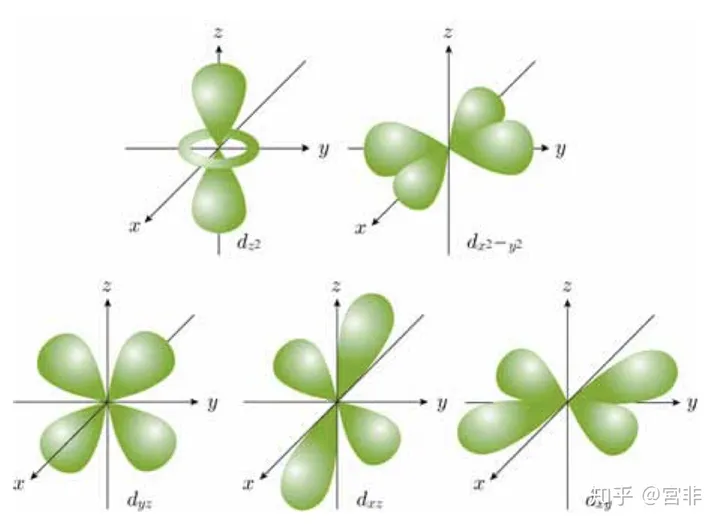
2.2.2 角量子数
决定了电子的轨道形状。
取值范围:
分别对应:
不同的轨道有不同的形状。
2.2.3 磁量子数
决定了轨道的方向。
取值范围:
注意:同一个
2.2.2.1
2.2.2.2
2.2.2.3
例题:
的轨道名称是什么?
2.2.4 自旋量子数
决定了这个电子在某个轨道上的“自转”方向。
取值只有两个:
2.3 泡利不相容原理
不存在
2.4 小补充
2.4.1 能级的排布
每个轨道的能量由
有时候,两个轨道的远近一样(
有时候,离核近的轨道反而能量更高,这就叫做能级交错,主要是因为受到了其他电子的排斥而能量增大。
如何准确地对各个能级进行排序呢?请见下节。
2.4.2 徐光宪近似规律
可以用来比较各个轨道能量的大小。
- 对于原子而言:
- 对于粒子而言:
2.4.3 能级的计算&屏蔽效应
- 对于单电子原子能级,有
- 对于多电子原子能级,有
其中,
为什么多电子原子能级要有减去
我们可以使用斯雷特规则来计算屏蔽常数
2.4.4 能级分裂的原因——钻穿效应
3 能级排布
3.1 能级排布规律图
由种种实验事实,人们总结出了一张图表,能帮助我们快速对能级进行排序。
由上图,我们可以看到,各个轨道的能量:
3.2 电子排布式
我们将电子依次填入能量低到能量高的轨道。其中,每个
接着,我们把放了多少个电子写到轨道的右上角。最后,我们还要将所有轨道按顺序排列。
以
而
但
3.3 洪特规则
- 尽可能成单电子排列且自旋方向相同。
- 简并轨道、全空、半满或全满比较稳定。

Preview: